- S3-Leitlinie Diagnostik, Therapie und Nachsorge des Mammakarzinoms. Version 4.1, September 2018. AWMF-Registernummer: 032-045OL. http://www.leitlinienprogramm-onkologie.de/leitlinien/mammakarzinom (Zugriff: 31.07.2019)
- Wörmann B et al. Mammakarzinom der Frau. Onkopedia-Leitlinie. Stand: Januar 2018. https://www.onkopedia.com/de/onkopedia/guidelines/mammakarzinom-der-frau/@@guideline/html/index.html (Zugriff am 31.07.2019)
- AGO Kommission Mamma. Diagnostik und Therapie früher und fortgeschrittener Mammakarzinome. (ago-online.de;Zugriff am 31.07.2019)
- Robert Koch-Institut und die Gesellschaft der epidemiologischen Krebsregister in Deutschland e. V. (Hrsg). Krebs in Deutschland 2011/2012. 10. Ausgabe. Berlin, 2015
- Hellriegel M et al. Endokrine Therapie des Mammakarzinoms. Frauenheilkunde up2date 2010;4(6):367-83. doi:10.1055/s-0030-1262695
- Jackisch C, Blohmer JU. S3-Leitlinie: Endokrine Therapie des primären Mammakarzinoms. Gynäkologe 2018;51:548-55. https://doi.org/10.1007/s00129-018-4276-7
- Banys-Paluchowski M et al. Aromatasehemmer: Eine kritische Bestandsaufnahme. Dtsch Arztebl 2016;113(11):[12]. doi:10.3238/PersGyn.2016.03.18.03
- Colleoni M et al. Extended adjuvant intermittent letrozole versus continuous letrozole in postmenopausal women with breast cancer (SOLE): a multicentre, open-label, randomised, phase 3 trial. Lancet Oncol 2018;19:127–38
- Davis C et al. Long-term effects of continuing adjuvant tamoxifen to 10 years versus stopping at 5 years after diagnosis of estrogen receptor-positive breast cancer: ATLAS, a randomized trial. Lancet 2013;381:805-16
- Gray RG et al. aTTom: Long-term effects of continuing adjuvant tamoxifen to 10 years versus stopping at 5 years in 6.953 women with early breast cancer. J Clin Oncol 2013;31(18_suppl):5-5. doi:10.1200/jco.2013.31.18_suppl.5
- Goss PE at al. Randomized trial of letrozole following tamoxifen as extended adjuvant therapy in receptor-positive breast cancer: updated findings from NCIC CTG MA.17. J Natl Cancer Inst 2005;97(17):1262-71
- Goss PE at al. Extending Aromatase-Inhibitor Adjuvant Therapy to 10 Years. N Engl J Med 2016;375(3):209-19. doi:10.1056/NEJMoa1604700
Wie sieht die optimale endokrine Therapie beim Mammakarzinom aus?
Es gibt – bei laufender wissenschaftlicher Diskussion und Forschung – eine ganze Reihe an evidenzbasierten Leitlinienempfehlungen, die den Weg zur optimalen endokrinen Therapie beim hormonsensitiven Mammakarzinom weisen – immer in Verbindung mit dem Blick auf Bedürfnisse und Adhärenz der Patientin.
Neben der Früherkennung tragen die Verbesserungen der Systemtherapie zum Anstieg der Überlebensraten bei Brustkrebs bei. Die endokrine Therapie stellt – als erster rezeptorgerichteter und damit „präzisionsmedizinischer“ Ansatz in der Onkologie – weiterhin den Grundpfeiler in der systemischen Behandlung des hormonsensitiven, HER2-negativen Mammakarzinoms dar. Deutsche Leitlinienempfehlungen dazu finden sich in der S3-Leitlinie1, der Onkopedia-Leitlinie2 und den im März dieses Jahres aktualisierten Folien der AGO Kommission Mamma3.
Effektivität korreliert mit dem quantitativen Hormonrezeptor-Nachweis
Demnach ist die adjuvante endokrine Therapie mit höchstem Empfehlungsgrad bei Patientinnen mit positivem Hormonrezeptorstatus ER und/oder PR (Östrogen- bzw. Progesteronrezeptor) des Primärtumors indiziert. Die Applikation beginnt erst nach Abschluss einer Chemotherapie, kann aber parallel zu einer Strahlentherapie erfolgen. Dabei ist zu berücksichtigen, dass die Effektivität der endokrinen Therapie klar mit dem quantitativen ER/PR-Nachweis korreliert1,3,6:
- 0 % positive Zellen: endokrin nicht sensitiv => keine endokrine Therapie;
- 1 – 9 % positive Zellen: endokrin fraglich sensitiv => endokrine Therapie (zusätzliche adjuvante oder neoadjuvante Chemotherapie zu erwägen);
- ≥ 10 % positive Zellen: endokrin sensitiv => endokrine Therapie.
Beachtenswert ist der AGO-Hinweis, dass der Status „ER negativ / PR positiv (≥ 10 % Zellen)“ nicht mehr als hormonrezeptor-positiv bewertet wird. Stattdessen ist in diesem Fall eine immunhistochemische Reevaluation erforderlich, da man festgestellt hat, dass die Bestimmung des Progesteronrezeptors häufig falsch positiv ausfällt.
Bei den jährlich rund 70.000 Neuerkrankungen in Deutschland4 handelt es sich in den meisten Fällen (75 – 85 %) um Tumore mit einer Überexpression nukleärer Östrogenrezeptoren5,6,7. Die größte antihormonelle therapeutische Relevanz kommt Tamoxifen und den Aromatasehemmern (AI) zu, von denen mit Anastrozol, Exemestan und Letrozol drei Vertreter der dritten Generation als Medikamente der ersten Wahl zur Verfügung stehen. Mit diesen adjuvanten endokrinen Therapien kann eine relative Risikoreduktion um ca. 40 % hinsichtlich Rezidiven und um ca. 30 % hinsichtlich der Mortalität erzielt werden, unabhängig von Patientenalter, Tumorstadium und Vortherapie.1
Wichtige Auswahlkriterien: Menopausenstatus und Rezidivrisiko
Wichtige Auswahlkriterien für die endokrine Therapie sind der Menopausenstatus und das individuelle Rückfallrisiko. Das Ausbleiben der Regelblutung allein ist kein verlässlicher Indikator für den postmenopausalen Status. Dieser ist gegeben bei
- Zustand nach beidseitiger Adnexexstirpation oder
- einem Alter über 60 Jahre oder
- fehlender Menstruation über ein Jahr sowie Östradiol- (E2-) und FSH-Werten im postmenopausalen Bereich.
Die zuverlässige Bestimmung des Menopausenstatus kann sich während einer Chemo- oder endokrinen Therapie etwas komplizierter gestalten und erfordert wiederholte Hormonbestimmungen, unter einer Behandlung mit GnRH-Analoga ist sie nicht möglich. Im Zweifelsfall sollte man sich an die Therapieempfehlungen für prämenopausale Patientinnen halten, bis die Menopause sicher erreicht ist.
Leitlinienempfehlungen kompakt
Zu den wichtigsten Praxisempfehlungen auf Leitlinienbasis zählen zusammengefasst u. a.:
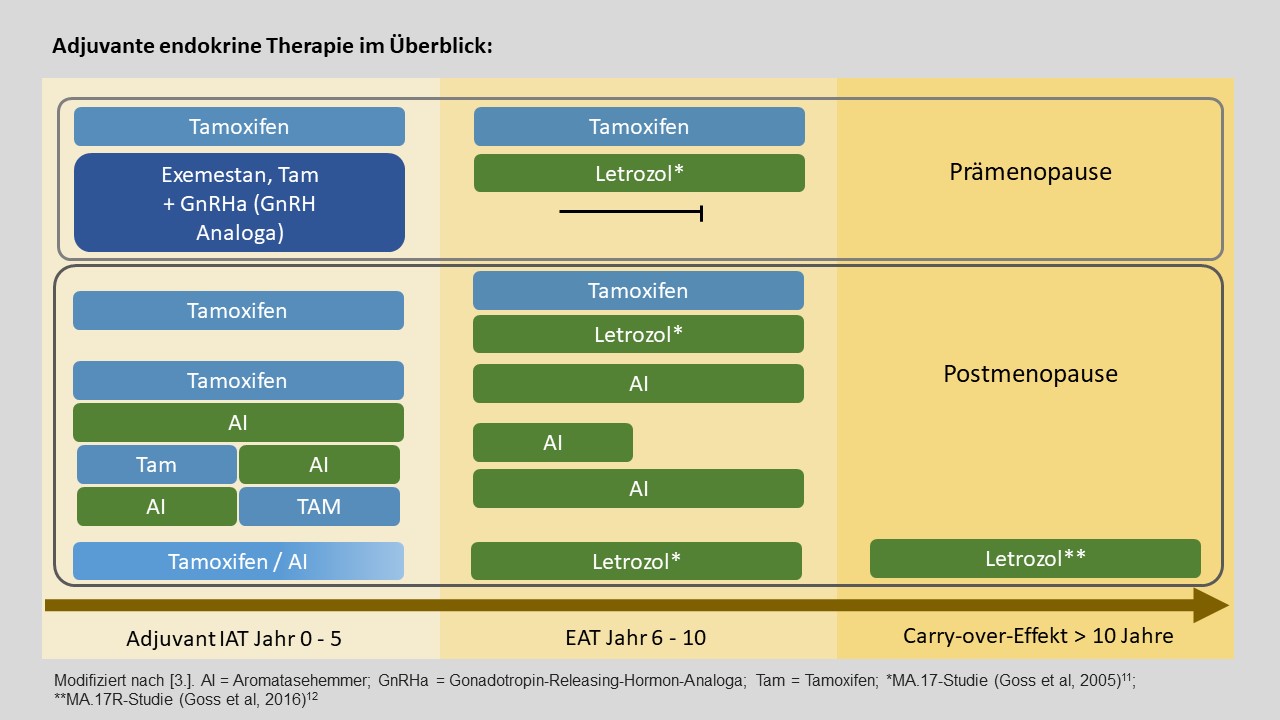
- Die endokrine Therapie wird in die initiale adjuvante Therapie (IAT; Jahre 0 –5) und die erweiterte adjuvante Therapie (EAT; Jahre 6 – 10, laut AGO: 6 – 15) eingeteilt, unabhängig vom Menopausenstatus.
- Auswahl, Dauer und Sequenz hängen v. a. von Menopausenstatus, Verträglichkeit und Rezidivrisiko ab. Die optimale Therapieform (Wirkstoffe, Länge) ist weiterhin Gegenstand der Forschung und Diskussion.
- Die Standarddauer der IAT beträgt 5 Jahre.
- Die EAT setzt nach Jahr 5 ein. Bei der Nutzen-Risiko-Abwägung zur Indikationsstellung sind u. a. das Rückfallrisiko und die therapieassoziierten Nebenwirkungen (Toxizität, verminderte Adhärenz) zu berücksichtigen.
- Bei einer IAT mit Tamoxifen über 5 Jahre ist eine anschließende EAT mit AI sinnvoll. Wurde bereits mit AI vorbehandelt, sollte eine EAT mit AI nur bei erhöhtem Risiko und guter Verträglichkeit erfolgen.
- Es gibt derzeit keinen ausreichend validierten Biomarker bzw. Multigen-Assay, um ein frühes oder spätes Rezidiv vorherzusagen.
- Die SOLE-Studie8 ergab zwar für die intermittierende Gabe von Letrozol gegenüber der kontinuierlichen Applikation keine Wirksamkeitsvorteile. Dafür wurde aber gezeigt, dass die endokrine Therapie für 3 Monate ohne Schaden für die Patientin unterbrochen werden kann.
- Behandlungsassoziierte Nebenwirkungen können die Therapieadhärenz stark beeinträchtigen und somit zu einem erheblichen Effektivitätsverlust führen. Deshalb gilt der Grundsatz: Besser eine Veränderung der Therapie (z. B. von einem AI auf Tamoxifen) als eine Beendigung der Therapie.
Prämenopause:
- Die Standardtherapie in der Prämenopause besteht in der Applikation von 20 mg/Tag Tamoxifen. Zur Ausschaltung der Ovarialfunktion bei hohem Rezidivrisiko nach adjuvanter Chemotherapie sollen begleitend GnRH-Analoga gegeben werden (im 28-Tage-Intervall, nicht als Dreimonatsspritze).
- Ist Tamoxifen kontraindiziert oder unerwünscht, kann eine alleinige Ovarialsuppression durch Behandlung mit GnRH-Analoga oder bilaterale Ovarektomie erfolgen.
- Die Tamoxifen-Therapie soll auf bis zu 10 Jahre verlängert werden, wenn die folgenden Kriterien zutreffen:
- erhöhtes Rezidivrisiko (z. B. bei N+ Status, Tumorgröße > 2 cm und histologischem Grading G3);
- weiterhin Prämenopausenstatus nach den ersten 5 Jahren der Therapie;
- gute Verträglichkeit der Tamoxifen-Therapie;
- Wunsch der Patientin.
- Studiendaten (ATLAS9; aTTom10) sprechen für reduzierte Rezidiv- und Sterblichkeitsraten bei verlängerter Behandlung mit Tamoxifen über 10 Jahre. Allerdings ist die prolongierte Einnahme auch mit einer erhöhten Anzahl an Lungenembolien und Endometriumkarzinomen assoziiert.
- Eine abschließende Bewertung für den Einsatz von AI (+ GnRHa) in der Prämenopause steht noch aus, ihr Einsatz bedarf einer sorgfältigen Abwägung und Aufklärung.
- Beim AI-Einsatz bei jungen Patientinnen mit chemotherapieinduzierter Amenorrhö (CIA) ist ein sicheres Monitoring der Ovarialfunktion (E2/FSH-Spiegel) unerlässlich. Der Grund: Bei bis zu 14 % (!) kommt es zu einer Wiederaufnahme der Ovarialfunktion.
- Bei potenziell noch bestehendem Kinderwunsch sollte auf den Erhalt der Ovarialfunktion geachtet und die Vorstellung in einem Reproduktionszentrum angeraten werden.
Postmenopause:
- In der Postmenopause sind risikoadaptiert Tamoxifen oder AI für 5 Jahre einzusetzen. Als Alternative kommt eine Sequenztherapie mit Tamoxifen gefolgt von AI oder umgekehrt in Frage.
- Ein Beginn mit AI in der Postmenopause wird insbesondere bei Hochrisiko-Patientinnen (z. B. N+) und lobulären Karzinomen empfohlen.
- Die IAT sollte einen AI für 2 – 3 Jahre beinhalten.
- Prämenopausale Patientinnen, die während der Tamoxifen-Therapie in die Postmenopause kommen, können von einer EAT mit AI profitieren.
- Eine höhere Adhärenz unter Tamoxifen ist effektiver als die Kombination AI + GnRH-Analogon bei eingeschränkter Adhärenz.
Selbstverständlich kann diese Auswahl an praxisrelevanten Hinweisen das Eigenstudium der Leitlinienempfehlungen nicht ersetzen. Bei all der „objektiven“ Informationsfülle darf ein Schlüsselfaktor für die Umsetzung der hochwirksamen adjuvanten endokrinen Therapien nicht übersehen werden: die Adhärenz.
Schlüsselfaktor: die Therapieadhärenz
Es wurde beobachtet, dass nach dem ersten Jahr der Einnahme 40 – 50 % der Patientinnen das verordnete Präparat absetzen, mit der Folge verminderter Raten des krankheitsfreien Überlebens und des Gesamtüberlebens.1 Die Adhärenz wird vor allem durch zwei Umstände gefährdet, die eine empathische und bewusstseinsfördernde Aufklärung im Rahmen der Verordnung zwingend erforderlich machen:
- Nebenwirkungen, die tatsächlich oder nur vermeintlich im Zusammenhang mit der Einnahme der Medikamente auftreten und
- die Notwendigkeit der langfristigen kontinuierlichen Einnahme.
Zu den Prädiktoren für einen Abbruch einer endokrinen Therapie zählen:
- ein niedrigeres und ein höheres Lebensalter (< 50 bzw. ≥ 75 Jahre);
- die brusterhaltende Therapie (versus Ablatio);
- bestehende Komorbiditäten (≥ 2);
- das Verschreiben von kleineren Packungsgrößen und höhere Zuzahlungen für Medikamente (insbesondere im höheren Lebensalter).
Als Prädiktoren für eine zuverlässige Einnahme haben sich dagegen die Ehe und eine durchgeführte Chemo- und Radiotherapie erwiesen.1
Auf das Thema Therapietreue sollte der behandelnde Gynäkologe in der Nachsorge detailliert und unter Berücksichtigung der Prädiktoren immer wieder eingehen, um die Adhärenz zu fördern und einen Abbruch der Einnahme sowie dessen Gründe erfahren und besprechen zu können. In der ärztlichen Dokumentation sollte dementsprechend nicht nur die Planung, sondern auch der tatsächliche Beginn, das Ende sowie die adäquate Durchführung der Therapie erfasst werden.
Laut Hinweisen aus Studiendaten gilt für die adjuvante endokrine Therapie: Besser spät als nie (bis zu 5 Jahre nach abgeschlossener Lokal- und/oder Chemotherapie) und lieber eine Therapiepause bei Nebenwirkungen als ein vollständiger Abbruch.1 Die optimale endokrine Therapie ist am Ende diejenige, die die Patientin auch tatsächlich beibehält.
Ajuvante endokrine Therapie mit Aristo – bewährt und kostengünstig:
Referenzen:
Abkürzungen:
AGO = Arbeitsgemeinschaft Gynäkologische Onkologie
AI = Aromatasehemmer (Aromataseinhibitoren)
CIA = chemotherapieinduzierte Amenorrhö
E2 = Östradiol
EAT = erweiterte adjuvante endokrine Therapie (Jahr 6 –10)
ER = Östrogenrezeptor
FSH = follikelstimulierendes Hormon
GnRH = Gonadotropin-Releasing-Hormon
HER2/neu = human epidermal growth factor receptor 2
IAT = initiale adjuvante endokrine Therapie (Jahr 0 –5)
N+ = Lymphknotenbefall
PR = Progesteronrezeptor